Гиперинсулинемия и выпадение волос
Содержание статьи
Дерматологические проявления инсулинорезистентности
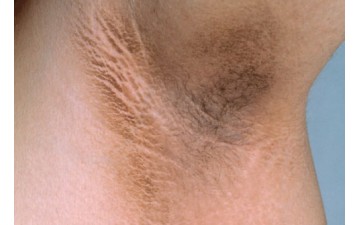
Сниженный биологической ответ ткани на воздействие нормальной концентрации инсулина называется инсулинорезистентностью (ИР). Организм вырабатывает инсулин (как правило, в более высоких концентрациях, чем у здоровых людей), но не использует его эффективно. Это один из ключевых патофизиологических факторов развития диабета 2 типа.
Резистентность к инсулину может проявляться в широком спектре дерматологических проявлений.
К ним относятся: черный акантоз, гирсутизм (яичниковая гиперандрогения), фиброэпителиальные полипы и андрогенетическая алопеция. Кожные проявления инсулинорезистентности в режиме реального времени помогают врачу определить дальнейшую тактику терапии, избежать диабета, повысить эффективность лечения метаболического синдрома, воздействовать на патогенез, а не бороться с симптомами. 91% пациентов с диабетом 2 типа имеют по крайней мере один дерматологический симптом. 70-80% пациентов с ожирением будет имеют резистентность к инсулину.
Инсулинорезистентность развивается за несколько лет до клинического диагноза сахарного диабета. Биологическое обоснование ассоциации ИР с кожными проявлениями опирается на тот факт, что гиперинсулинемия активирует рецепторы к инсулиноподобному фактору роста-1 (ИФР-1), расположенных в фибробластах и кератиноцитах. Повышенный уровень инсулина и ИФР-1 увеличивают выработку андрогенов в яичниках через повышение местной активности 17-гидроксилазы и ингибирования печеночного синтеза секс-гормон-связывающего глобулина (shbg), что повышает доступность свободного тестостерона.
Андрогенетическая алопеция. Одним из распространенных факторов андрогенетической алопеции (АГА) является метаболический синдром (включающий инсулинорезистентность). Тестостерон метаболизируется во многих тканях кожи. Он проникает через клеточную мембрану и необратимо преобразовывается с помощью 5-Альфа-редуктазы (преимущественно II типа) в цитоплазме в наиболее мощной форму: дигидротестостерон (ДГТ). ДГТ является основным андрогеном, участвующим в патогенезе АГА. ДГТ связывается с рецепторами андрогенов и транслоцируется в ядро, где стимулирует транскрипцию гена. Эта активация является ключом к постепенной трансформации терминальных фолликулов в небольшие пушковые волосики, с укороченного анагена.
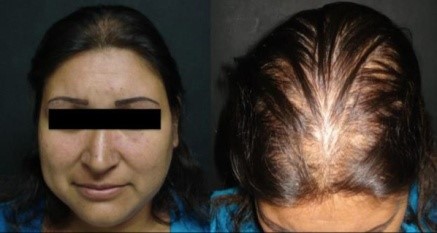
Потеря волос по женскому типу.
Другие кожные проявления. Фиброэпителиальная полипы. ИФР-1 связывается с рецепторами в кератиноцитах, вызывая эпидермальную гиперплазию. Клинически это маленькие, мягкие, слегка гиперпигментированные опухоли различного размера, имеющие ножку. Часто множественные, но могут проявиться как единичное поражение. Шея, подмышечные впадины и пах являются наиболее распространенными областями поражения, однако, поражаться могут веки и в подгрудные складки.
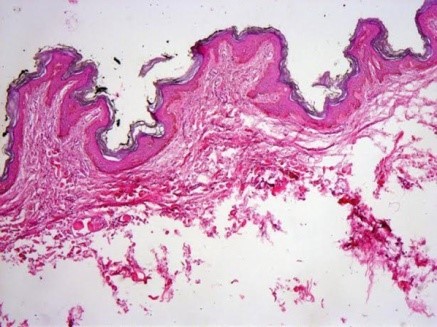
Гистологическая картина, демонстрирующая папилломатоз.
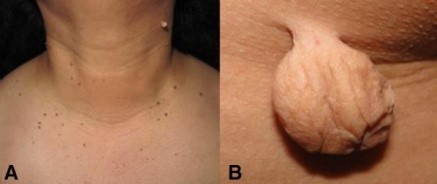
Клиническая картина.
Черный акантоз. Чаще всего является признаком инсулинорезистентности, однако существуют и другие причины развития. Доброкачественный вариант врожденный или развивается в раннем детстве. Не связан с метаболическими изменениями. Злокачественная форма ассоциируется с аденокарциномой желудочно-кишечного тракта. Ассоциированный с приемом лекарственных средств, таких как никотиновая кислота, оральные контрацептивы, кортикостероиды, и метилтестостерон. Как правило, проходит самопроизвольно в течение 4-11 месяцев после прекращения приема препарата. Ожирение-связанный является наиболее частым вариантом и развивается как проявление резистентности к инсулину. Патогенез аналогичен папилломатозу (результат стимуляции ИФР-1 кератиноцитов и фибробластов в дерме). Классический топография включает в себя шею, подмышечные впадины и локти Возможно проявление в периорбитальной и околопупочной областях, внутренней поверхности бедер, подгрудной складки, коленях.
Гирсутизм, акне. Термин «диабет бородатых женщин» был использован впервые Арчард и Тьер в 1920-е годы, когда впервые выявлена взаимосвязь нарушения углеводного обмена и гиперандрогении. Синдром поликистозных яичников (СПКЯ) является общепризнанным метаболическим изменением, связанным с повышенным риском развития СД-2 и бесплодия. Независимо от ожирения, большой процент женщины с СПКЯ имеют резистентность к инсулину. Распространенность ожирения среди них колеблется от 25% до 70% (обычно центральный тип) и способствует инсулинорезистентности. В пробирке исследования показали, что инсулин усиливает действие лютоинезирующего гормона на яичниковую продукции андрогенов . Гиперандрогения является одним из ключевых диагностических признаков СПКЯ и проявляется клинически как гирсутизм, акне и АГА.
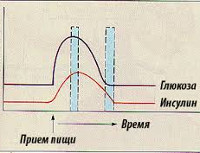
Диагностика. Тест толерантности к глюкозе считается золотым стандартом для диагностики инсулинорезистентности. Он выявляет повышение сахара натощак а так же после еды.
Примечание: Однако ИР может развиться задолго до повышения сахара в крови. Для ее выявления на ранних стадиях возможно проведение теста толерантности к глюкозе с определением не только сахара, но и С-пептида, инсулина. Повышение С-пептида и инсулина говорят о их повышенной продукции для преодоления тканевого сопротивления.
Лечение. Методы преодоления инсулинорезистентности включают в себя модификацию образа жизни, питания и медикаментозную терапию. Изменение образа жизни должно включать физические упражнения и потерю веса. Инсулин-сенсибилизирующие средства, такие как метформин.
Примечание: При выставленном диагнозе «сахарный диабет 2 типа», рекомендуемая доза метформина 2000-3000 мг в сутки. Старт терапии с 500мг в сутки, с дальнейшим увеличением дозы по 500мг через 1-2 недели. При выявлении инсулинорезистентности без повышения гликемии рекомендуемая доза 1000мг с контролем инсулина и С-пептида. При отсутствии нормализации этих показателей возможно повышение дозы.
Вернуться назад
Источник
Обратима ли резистентность к инсулину?
Эндокринологи утверждают, что резистентность к инсулину можно предотвратить, и даже обратить вспять. Для это требуется особая диета и полное изменение образа жизни под наблюдением врача.
Что такое инсулинорезистентность
С инсулинорезистентностью, клетки становятся нечувствительными к инсулину, поэтому для поддержания уровня глюкозы в крови его требуется все больше.
Высокий уровень инсулина усиливает аппетит, что приводит к дополнительному потреблению углеводов и увеличению веса. Возникают и другие осложнения, например, повышается давление, сбивается менструальный цикл, ухудшается общее состояние.
Прекратить этот порочный круг нужно как можно раньше, прежде чем разовьется диабет и осложнения перейдут черту невозврата.
Как справиться с резистентностью к инсулину
Вероятность вылечиться зависит от многих факторов:
- Степень развития резистентности к инсулину. Процесс легче изменить при условии, что резистентность клеток к инсулину низкая, но инсулин все еще вырабатывается должным образом, т.е. в организме не произошло значительных изменений;
- Продолжительность патологии. Чем раньше диагностирована проблема, тем выше вероятность ее разрешения;
- Количество и степень осложнений. Большое значение имеет, например, степень связи резистентности к инсулину с ожирением;
- Сопутствующие заболевания. Ситуацию осложняют гипертония, подагра, метаболический синдром, ожирение печени, возраст. Шансы на выздоровление и эффективность терапии выше в у молодых пациентов;
- Наследственные факторы;
- Воля, дисциплинированность и решимость пациента. Это один из основных факторов успешного излечения.
Что нужно сделать, чтобы изменить резистентность к инсулину?
- Изменение привычек питания;
- Полное изменение образа жизни, включая выполнение лечебной физкультуры;
- Грамотное медикаментозное лечение.
Каких результатов можно ожидать, если приложить все усилия?
При эффективном лечении можно ожидать значительного улучшения и устранения возникших симптомов и осложнений. Хотя инсулинорезистентность сама по себе не обязательно вызывает симптомы, но если они есть, с ними вполне можно справиться.
Остановить можно:
- увеличение веса;
- выпадение волос;
- усиленный рост волос, связанный с избыточной выработкой андрогенных гормонов;
- повышенный аппетит и жажду;
- нервозность, усталость, напряжение.
Увеличение веса
Выпадение волос
Также улучшается ситуация:
- с повышенным давлением;
- ожирением печени;
- рядом кожных симптомов.
Сегодня проблемы с инсулинорезистентностью имеют даже подростки и женщины детородного возраста. Правильное лечение избавляет от гормональных нарушений, сбоя менструального цикла, синдрома поликистозных яичников и бесплодия.
Может ли исчезнуть резистентность к инсулину?
Да. Изменения в образе жизни, правильное питание, регулярные физические упражнения и, при необходимости, медикаментозное лечение могут снизить резистентность к инсулину.
Многочисленные международные исследования показали, что обратимость процесса возможна даже в некоторых случаях недавно диагностированного диабета 2 типа. Помимо нормализации выработки инсулина, улучшается реакция клеток на инсулин, а это означает, что для поглощения глюкозы снова требуется его более низкий уровень.
Конечно, этот процесс может быть обращен вспять только в течение определенного периода времени, пока выработка панкреатического инсулина идет удовлетворительными темпами, особенно в случаях раннего выявления, без осложнений или сопутствующих заболеваний.
Лечение инсулинрезистентности
На основании проведенных к настоящему времени исследований, для лечения преддиабета был разрешен метформин. Его можно использовать в отдельных случаях у пациентов с высоким риском развития диабета по соответствующим показаниям.
![]() Метформин
Метформин
При преддиабете метформин снижает риск развития диабета. Тем не менее, исследования показывают, что гораздо важнее в профилактике диабета изменение образа жизни. Терапия образа жизни — это прежде всего потеря веса, здоровое питание и регулярные физические упражнения Эти методы улучшают чувствительность тканей к инсулину, снижают нагрузку на поджелудочную железу и останавливают процесс.
- При соблюдении диеты следует соблюдать осторожность. Важно следовать личным советам эндокринолога. План питания должен включать снижение потребления углеводов и жиров и обеспечение их равномерного распределения.
- В случае избыточного веса, необходима нормализация массы тела, но потеря веса не должна строиться на радикальной диете, подразумевающей голодание.
- Благотворное влияние на массу тела и общий обмен веществ оказывают регулярные физические упражнения 3-4 раза в неделю. Повышают чувствительность тканей к инсулину тренировки для укрепления сердечно-сосудистой системы и мышц.
- Среди диетических добавок полезны инозитол, витамины группы В.
Во время лечения важно следить за заболеванием, проводя регулярные контрольные анализы на глюкозу, сахар. При метаболических отклонениях показателей проводится корректировка назначений.
Терапия должна включать лечение сопутствующих заболеваний, например, СПКЯ, нарушений работы щитовидной железы, высокий уровень холестерина.
Важное значение имеет начало медикаментозного лечения, если резистентность к инсулину переходит к следующей фазе углеводного обмена, Целевое значение для каждой фазы лечения составляет <7% HbA1C. Если используемая терапия не дает желаемого уровня глюкозы в крови через 3 месяца, направление лечения должно быть изменено.
Источник
Биология волос
2.5. Инсулин и инсулиноподобные факторы роста
Инсулин — гормон пептидной природы, образуется в бета-клетках островков Лангерганса поджелудочной железы. Основное действие инсулина заключается в снижении концентрации глюкозы в крови. Инсулин увеличивает проницаемость плазматических мембран для глюкозы, активирует ключевые ферменты гликолиза, стимулирует образование в печени и мышцах из глюкозы гликогена, усиливает синтез жиров и белков.
Кроме того, инсулин подавляет активность ферментов, расщепляющих гликоген и жиры. То есть, помимо анаболического действия, инсулин обладает также и антикатаболическим эффектом. Нарушение секреции инсулина вследствие деструкции бета-клеток — абсолютная недостаточность инсулина — является ключевым звеном патогенеза сахарного диабета 1-го типа. Нарушение действия инсулина на ткани — относительная инсулиновая недостаточность — имеет важное место в развитии сахарного диабета 2-го типа.
В исследовании Philpott M.P. с соавт. (1994) показано, что инсулин является стимулятором роста волос in vitro в диапазоне концентраций 0,01-100 мкг/мл. Максимальные темпы роста волосяного фолликула наблюдались при концентрации инсулина 10 мкг/мл. Волосяные фолликулы в отсутствие инсулина или при его физиологических уровнях преждевременно входили в фазу катагена. Инсулиноподобные факторы роста IGF-I и IGF-II не производили значимого эффекта на рост волосяного фолликула в присутствии 10 мкг/мл инсулина. Однако картина менялась, если инсулин отсутствовал, — в этом случае IGF-I и IGF-II стимулировали рост волосяного фолликула. При этом IGF-I становится даже более мощным фактором роста, чем сам инсулин.
В клинической практике стоит обратить внимание на связь андрогенетической алопеции с метаболическим синдромом, ключевую роль в развитии которого имеет избыточная секреция инсулина на фоне низкой чувствительности клеток к этому гормону. Впервые этот синдром описал американский ученый Джеральд Ривен. В конце 1980-х гг. Ривен обосновал существование синдрома резистентности к инсулину, определяющего сопутствующее развитие артериальной гипертензии, сахарного диабета 2-го типа, дислипидемии и атеросклероза.
В 2003 г. опубликованы данные популяционного исследования, проведенного финскими исследователями: женщины с алопецией 2-3-й стадии по Людвигу достоверно чаще имели признаки инсулинорезистентности (висцеральное ожирение, уровень инсулина свыше 10 mU/l, микроальбуминурия) в сравнении с контрольной группой. Сделан вывод, что женщины с маркерами инсулинорезистентности подвержены значимым рискам развития алопеции (Matilainen V., et al., 2003).
Спустя 3 года работа была продолжена, на этот раз в исследовании участвовало 245 мужчин в возрасте 63 года. Анализ данных показал, что достоверно чаще облысение имели мужчины, у которых диагностирована артериальная гипертензия. Гиперинсулинемия и инсулинорезистентность диагностированы у 61% мужчин с андрогенетической алопецией против 49% без алопеции.
Еще более убедительные данные показаны в исследовании Ahouansou S.A. с соавт. (2007), выявившем аналогичную взаимосвязь, — 82% мужчин с артериальной гипертензией имели облысение, в то время как в группе с нормальным артериальным давлением алопеция отмечалась у 56%.
Достоверная корреляция между андрогенетической алопецией у женщин и наличием коронарной патологии, часто развивающейся на фоне инсулинорезистентности, показана в исследовании Mansouri P. с соавт. (2005).
Была отмечена связь между повышенной активностью 5α-редуктазы и резистентностью к инсулину как у мужчин, так и у женщин (Tomlinson J.W., et al., 2008).
Хорошо известно, что у женщин инсулинорезистентность имеет выраженную ассоциацию с синдромом поликистозных яичников (наиболее частая причина функциональной гиперандрогении у женщин), при котором, помимо системной гиперандрогении, ановуляции, метаболических нарушений, отмечается избыточная активность 5α-редуктазы и, как правило, присутствует андрогенная алопеция, акне и гирсутизм (рис. I-2-3) (Burghen G.A., et al., 1980; Dunaif A., Hoffman A.R., 1988; Tsilchorozidou H., et al., 2002).
Рис. I-2-3. Связь инсулинорезистентности и гиперандрогении
Страница 5 — 5 из 8
Начало | Пред. | 3 4 5 6 7 | След. | Конец | Все
Источник
Гиперинсулинизм
Гиперинсулинизм — клинический синдром, характеризующийся повышением уровня инсулина и снижением сахара в крови. Гипогликемия приводит к слабости, головокружению, повышению аппетита, тремору, психомоторному возбуждению. При отсутствии своевременного лечения развивается гипогликемическая кома. Диагностика причин состояния основывается на особенностях клинической картины, данных функциональных проб, динамическом исследовании глюкозы, ультразвуковом или томографическом сканировании поджелудочной железы. Лечение панкреатических новообразований — хирургическое. При внепанкреатическом варианте синдрома проводят терапию основного заболевания, назначают специальную диету.
Общие сведения
Гиперинсулинизм (гипогликемическая болезнь) — врожденное или приобретенное патологическое состояние, при котором развивается абсолютная или относительная эндогенная гиперинсулинемия. Признаки болезни впервые были описаны в начале ХХ века американским врачом Харрисом и отечественным хирургом Оппелем. Врожденный гиперинсулинизм встречается достаточно редко — 1 случай на 50 тыс. новорожденных. Приобретенная форма заболевания развивается в возрасте 35-50 лет и чаще поражает лиц женского пола. Гипогликемическая болезнь протекает с периодами отсутствия выраженной симптоматики (ремиссия) и с периодами развернутой клинической картины (приступы гипогликемии).
Гиперинсулинизм
Причины гиперинсулинизма
Врожденная патология возникает вследствие внутриутробных аномалий развития, задержки роста плода, мутаций в геноме. Причины возникновения приобретенной гипогликемической болезни разделяют на панкреатические, приводящие к развитию абсолютной гиперинсулинемии, и непанкреатические, вызывающие относительное повышение уровня инсулина. Панкреатическая форма болезни встречается при злокачественных или доброкачественных новообразованиях, а также гиперплазии бета-клеток поджелудочной железы. Непанкреатическая форма развивается при следующих состояниях:
- Нарушения в режиме питания. Длительное голодание, повышенная потеря жидкости и глюкозы (поносы, рвота, период лактации), интенсивные физические нагрузки без потребления углеводной пищи вызывают резкое снижение уровня сахара в крови. Чрезмерное употребление в пищу рафинированных углеводов увеличивает уровень сахара крови, что стимулирует активную выработку инсулина.
- Поражение печени различной этиологии (рак, жировой гепатоз, цирроз) приводит к снижению уровня гликогена, нарушению обменных процессов и возникновению гипогликемии.
- Бесконтрольный прием сахароснижающих препаратов при сахарном диабете (производных инсулина, сульфанилмочевины) вызывает медикаментозную гипогликемию.
- Эндокринные заболевания, приводящие к снижению уровня контринсулиновых гормонов (АКТГ, кортизол): гипофизарный нанизм, микседема, болезнь Аддисона.
- Недостаток ферментов, участвующих в процессах обмена глюкозы (печеночная фосфорилаза, почечная инсулиназа, глюкозо-6-фосфатаза) вызывает относительный гиперинсулинизм.
Патогенез
Глюкоза является главным питательным субстратом центральной нервной системы и необходима для нормального функционирования головного мозга. Повышенный уровень инсулина, накопление гликогена в печени и торможение гликогенолиза приводит к снижению уровня глюкозы в крови. Гипогликемия вызывает торможение метаболических и энергетических процессов в клетках головного мозга. Происходит стимуляция симпатоадреналовой системы, увеличивается выработка катехоламинов, развивается приступ гиперинсулинизма (тахикардия, раздражительность, чувство страха). Нарушение окислительно-восстановительных процессов в организме приводит к снижению потребления кислорода клетками коры головного мозга и развитию гипоксии (сонливость, заторможенность, апатия). Дальнейший дефицит глюкозы вызывает нарушение всех обменных процессов в организме, увеличение притока крови к мозговым структурам и спазм периферических сосудов, что может привести к инфаркту. При вовлечении в патологический процесс древних структур мозга (продолговатый и средний мозг, варолиев мост) развиваются судорожные состояния, диплопия, а также нарушение дыхательной и сердечной деятельности.
Классификация
В клинической эндокринологии наиболее часто используется классификация гиперинсулинемии в зависимости от причин возникновения заболевания:
- Первичный гиперинсулинизм (панкреатический, органический, абсолютный) является следствием опухолевого процесса или гиперплазии бета-клеток островкового аппарата поджелудочной железы. Повышению уровня инсулина в 90% способствуют доброкачественные новообразования (инсулинома), реже — злокачественные (карцинома). Органическая гиперинсулинемия протекает в тяжелой форме с выраженной клинической картиной и частыми приступами гипогликемии. Резкое понижение уровня сахара в крови возникает утром, связано с пропуском приема пищи. Для данной формы заболевания характерна триада Уиппла: симптомы гипогликемии, резкое снижение сахара в крови и купирование приступов введением глюкозы.
- Вторичный гиперинсулинизм (функциональный, относительный, внепанкреатический) связан с дефицитом контринсулярных гормонов, поражением нервной системы и печени. Приступ гипогликемии возникает по внешним причинам: голодание, передозировка гипогликемических препаратов, интенсивная физическая нагрузка, психоэмоциональное потрясение. Обострения болезни возникают нерегулярно, практически не связаны с приемом пищи. Суточное голодание не вызывает развернутой симптоматики.
Симптомы гиперинсулинизма
Клиническая картина гипогликемической болезни обусловлена понижением уровня глюкозы в крови. Развитие приступа начинается с повышения аппетита, потливости, слабости, тахикардии и ощущения голода. Позже присоединяются панические состояния: чувство страха, тревога, раздражительность, дрожь в конечностях. При дальнейшем развитии приступа отмечается дезориентация в пространстве, диплопия, парестезии (онемение, покалывание) в конечностях, вплоть до возникновения судорог. При отсутствии лечения наступает потеря сознания и гипогликемическая кома. Межприступный период проявляется снижением памяти, эмоциональной лабильностью, апатией, нарушением чувствительности и онемением в конечностях. Частый прием пищи, богатой легкоусвояемыми углеводами, провоцирует увеличение массы тела и развитие ожирения.
В современной практике выделяют 3 степени гиперинсулинизма в зависимости от тяжести течения болезни: легкую, среднюю и тяжелую. Легкая степень проявляется отсутствием симптоматики межприступного периода и органического поражения коры головного мозга. Обострения болезни проявляются реже 1 раза в месяц и быстро купируются медикаментозными препаратами или сладкой пищей. При средней степени тяжести приступы возникают чаще 1 раза в месяц, возможна потеря сознания и развитие коматозного состояния. Межприступный период характеризуется легкими нарушениями поведенческого характера (забывчивость, снижение мышления). Тяжелая степень развивается при необратимых изменениях коры головного мозга. При этом приступы случаются часто и заканчиваются потерей сознания. В межприступном периоде пациент дезориентирован, память резко снижена, отмечается тремор конечностей, характерна резкая смена настроения и повышенная раздражительность.
Осложнения гиперинсулинизма
Осложнения можно условно разделить на ранние и поздние. К ранним осложнениям, возникающим в ближайшие часы после приступа, относят инсульт, инфаркт миокарда вследствие резкого снижения метаболизма сердечной мышцы и головного мозга. В тяжелых ситуациях развивается гипогликемическая кома. Поздние осложнения проявляются спустя несколько месяцев или лет от начала болезни и характеризуются нарушением памяти и речи, паркинсонизмом, энцефалопатией. Отсутствие своевременного диагностики и лечения заболевания приводит к истощению эндокринной функции поджелудочной железы и развитию сахарного диабета, метаболического синдрома, ожирения. Врожденный гиперинсулинизм в 30% случаев приводит к хронической гипоксии головного мозга и снижению полноценного умственного развития ребенка.
Диагностика гиперинсулинизма
Диагностика основывается на клинической картине (потеря сознания, тремор, психомоторное возбуждение), данных анамнеза заболевания (время начала приступа, его связь с приемом пищи). Эндокринолог уточняет наличие сопутствующих и наследственных заболеваний (жировой гепатоз, сахарный диабет, синдром Иценко-Кушинга), после чего назначает лабораторные и инструментальные исследования. Пациенту проводится суточное измерение уровня глюкозы крови (гликемический профиль). При выявлении отклонений выполняют функциональные пробы. Проба с голоданием используется для дифференциальной диагностики первичного и вторичного гиперинсулинизма. Во время теста измеряют С-пептид, иммунореактивный инсулин (ИРИ) и глюкозу в крови. Повышение данных показателей свидетельствует об органическом характере болезни.
Для подтверждения панкреатической этиологии заболевания проводят тесты на чувствительность к толбутамиду и лейцину. При положительных результатах функциональных проб показано УЗИ, сцинтиграфия и МРТ поджелудочной железы. При вторичном гиперинсулинизме для исключения новообразований других органов выполняют УЗИ брюшной полости, МРТ головного мозга. Дифференциальная диагностика гипогликемической болезни проводится с синдромом Золлингера-Эллисона, началом развития сахарного диабета 2 типа, неврологическими (эпилепсия, новообразования головного мозга) и психическими (неврозоподобные состояния, психоз) заболеваниями.
Лечение гиперинсулинизма
Тактика лечения зависит от причины возникновения гиперинсулинемии. При органическом генезе показано хирургическое лечение: частичная резекция поджелудочной железы или тотальная панкреатэктомия, энуклеация новообразования. Объем оперативного вмешательства определяется местоположением и размерами опухоли. После операции обычно отмечается транзиторная гипергликемия, требующая медикаментозной коррекции и диеты с пониженным содержанием углеводов. Нормализация показателей наступает через месяц после вмешательства. При неоперабельных опухолях проводят паллиативную терапию, направленную на профилактику гипогликемии. При злокачественных новообразованиях дополнительно показана химиотерапия.
Функциональный гиперинсулинизм в первую очередь требует лечения основного заболевания, вызвавшего повышенную продукцию инсулина. Всем больным назначается сбалансированная диета с умеренным снижением потребления углеводов (100-150 гр. в сутки). Отдается предпочтение сложным углеводам (ржаные хлебцы, макароны из твердых сортов пшеницы, цельнозерновые крупы, орехи). Питание должно быть дробным, 5-6 раз в день. В связи с тем, что периодические приступы вызывают у пациентов развитие панических состояний, рекомендована консультация психолога. При развитии гипогликемического приступа показано употребление легкоусвояемых углеводов (сладкий чай, конфета, белый хлеб). При отсутствии сознания необходимо внутривенное введение 40 % раствора глюкозы. При судорогах и выраженном психомоторном возбуждении показаны инъекции транквилизаторов и седативных препаратов. Лечение тяжелых приступов гиперинсулинизма с развитием комы осуществляют в условиях реанимационного отделения с проведением дезинтоксикационной инфузионной терапии, введением глюкокортикоидов и адреналина.
Прогноз и профилактика
Профилактика гипогликемической болезни включает в себя сбалансированное питание с интервалом в 2-3 часа, употребление достаточного количества питьевой воды, отказ от вредных привычек, а также контроль уровня глюкозы. Для поддержания и улучшения обменных процессов в организме рекомендованы умеренные физические нагрузки с соблюдением режима питания. Прогноз при гиперинсулинизме зависит от стадии заболевания и причин, вызывавших инсулинемию. Удаление доброкачественных новообразований в 90% случаев обеспечивают выздоровление. Неоперабельные и злокачественные опухоли вызывают необратимые неврологические изменения и требуют постоянного контроля за состоянием пациента. Лечение основного заболевания при функциональном характере гиперинсулинемии приводит к регрессии симптомов и последующему выздоровлению.
Источник